ЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых проводят электрический ток.
НЕЭЛЕКТРОЛИТЫ – вещества, растворы или расплавы которых не проводят электрический ток.
Диссоциация – распад соединений на ионы.
Степень диссоциации – отношение числа продиссоциированных на ионы молекул к общему числу молекул в растворе.
СИЛЬНЫЕ ЭЛЕКТРОЛИТЫ при растворении в воде практически полностью диссоциируют на ионы.
При написании уравнений диссоциации сильных электролитов ставят знак равенства.
К сильным электролитам относятся:
· Растворимые соли (смотри таблицу растворимости );
· Многие неорганические кислоты: HNO 3 , H 2 SO 4 ,HClO 3 , HClO 4 , HMnO 4 , HCl, HBr, HI (смотри кислоты-сильные электролиты в таблице растворимости );
· Основания щелочных (LiOH, NaOH,KOH) и щелочноземельных (Ca(OH) 2 , Sr(OH) 2 , Ba(OH) 2) металлов (смотри основания-сильные электролиты в таблице растворимости ).
СЛАБЫЕ ЭЛЕКТРОЛИТЫ в водных растворах лишь частично (обратимо) диссоциируют на ионы.
При написании уравнений диссоциации слабых электролитов ставят знак обратимости.
К слабым электролитам относятся:
· Почти все органические кислоты и вода (Н 2 О);
· Некоторые неорганические кислоты: H 2 S, H 3 PO 4 ,HClO 4 , H 2 CO 3 , HNO 2 , H 2 SiO 3 (смотри кислоты-слабые электролиты в таблице растворимости );
· Нерастворимые гидроксиды металлов (Mg(OH) 2 ,Fe(OH) 2 , Zn(OH) 2) (смотри основания- c лабые электролиты в таблице растворимости ).
На степень электролитической диссоциации влияет ряд факторов:
природа растворителя и электролита : сильными электролитами являются вещества с ионными и ковалентными сильно-полярными связями; хорошей ионизирующей способностью, т.е. способностью вызывать диссоциацию веществ, обладают растворители с большой диэлектрической проницаемостью, молекулы которых полярны (например, вода);
температура : поскольку диссоциация - процесс эндотермический, повышение температуры повышает значение α;
концентрация : при разбавлении раствора степень диссоциации возрастает, а с увеличением концентрации - уменьшается;
стадия процесса диссоциации : каждая последующая стадия менее эффективна, чем предыдущая, примерно в 1000–10 000 раз; например, для фосфорной кислоты α 1 > α 2 > α 3:
H3PО4⇄Н++H2PО−4 (первая стадия, α 1),
H2PО−4⇄Н++HPО2−4 (вторая стадия, α 2),
НPО2−4⇄Н++PО3−4 (третья стадия, α 3).
По этой причине в растворе данной кислоты концентрация ионов водорода наибольшая, а фосфат-ионов РО3−4 - наименьшая.
1. Растворимость и степень диссоциации вещества между собой не связаны. Например, слабым электролитом является хорошо (неограниченно) растворимая в воде уксусная кислота.
2. В растворе слабого электролита меньше других содержится тех ионов, которые образуются на последней стадии электролитической диссоциации
На степень электролитической диссоциации влияет также добавление других электролитов : например, степень диссоциации муравьиной кислоты
HCOOH ⇄ HCOO − + H +
уменьшается, если в раствор внести немного формиата натрия. Эта соль диссоциирует с образованием формиат-ионов HCOO − :
HCOONa → HCOO − + Na +
В результате в растворе концентрация ионов НСОО– повышается, а согласно принципу Ле Шателье, повышение концентрации формиат-ионов смещает равновесие процесса диссоциации муравьиной кислоты влево, т.е. степень диссоциации уменьшается.
Закон разбавления Оствальда - соотношение, выражающее зависимость эквивалентной электропроводностиразбавленного раствора бинарного слабого электролита от концентрации раствора:
Здесь - константа диссоциации электролита, - концентрация, и - значения эквивалентной электропроводности при концентрации и при бесконечном разбавлении соответственно. Соотношение является следствием закона действующих масс и равенства
где - степень диссоциации.
Закон разбавления Оствальда выведен В.Оствальдом в 1888 году и им же подтвержден опытным путём. Экспериментальное установление правильности закона разбавления Оствальда имело большое значение для обоснования теории электролитической диссоциации.
Электролитическая диссоциация воды. Водородный показатель рН Вода представляет собой слабый амфотерный электролит: Н2О Н+ + ОН- или, более точно: 2Н2О= Н3О+ + ОН- Константа диссоциации воды при 25оС равна: Такое значение константы соответствует диссоциации одной из ста миллионов молекул воды, поэтому концентрацию воды можно считать постоянной и равной 55,55 моль/л (плотность воды 1000 г/л, масса 1 л 1000 г, количество вещества воды 1000г:18г/моль=55,55 моль, С=55,55 моль: 1 л =55,55 моль/л). Тогда Эта величина постоянная при данной температуре (25оС), она называется ионным произведением воды KW: Диссоциация воды – процесс эндотермический, поэтому с повышением температуры в соответствии с принципом Ле-Шателье диссоциация усиливается, ионное произведение возрастает и достигает при 100оС значения 10-13. В чистой воде при 25оС концентрации ионов водорода и гидроксила равны между собой: = = 10-7 моль/л Растворы, в которых концентрации ионов водорода и гидроксила равны между собой, называются нейтральными. Если к чистой воде прибавить кислоту, концентрация ионов водорда повысится и станет больше, чем 10-7 моль/л, среда станет кислой, при этом концентрация ионов гидроксила мгновенно изменится так, чтобы ионное произведение воды сохранило свое значение 10-14. Тоже самое будет происходить и при добавлении к чистой воде щелочи. Концентрации ионов водорода и гидроксила связаны между собой через ионное произведение, поэтому, зная концентрацию одного из ионов, легко вычислить концентрацию другого. Например, если = 10-3 моль/л, то = KW/ = 10-14/10-3 = 10-11 моль/л, или, если = 10-2 моль/л, то = KW/ = 10-14/10-2 = 10-12 моль/л. Таким образом, концентрация ионов водорода или гидроксила может служить количественной характеристикой кислотности или щелочности среды. На практике пользуются не концентрациями ионов водорода или гидроксила, а водородным рН или гидроксильным рОН показателями. Водородный показатель рН равен отрицательному десятичному логарифму концентрации ионов водорода: рН = - lg Гидроксильный показатель рОН равен отрицательному десятичному логарифму концентрации ионов гидроксила: рОН = - lg Легко показать, прологарифмировав ионное произведение воды, что рН + рОН = 14 Если рН среды равен 7 - среда нейтральная, если меньше 7 - кислая, причем чем меньше рН, тем выше концентрация ионов водорода. pН больше 7 – среда щелочная, чем больше рН, тем выше концентрация ионов гидроксила.
, , 21 , , ,
, 25-26 , 27-28 ,
, 30, , , , , , , , /2003
§ 6.3. Сильные и слабые электролиты
Материал этого раздела частично вам знаком по ранее изученным школьным курсам химии и из предыдущего раздела. Кратко повторим, что вам известно, и познакомимся с новым материалом.
В предыдущем разделе мы обсуждали поведение в
водных растворах некоторых солей и органических
веществ, полностью распадающихся на ионы в
водном растворе.
Имеется ряд простых, но несомненных
доказательств того, что некоторые вещества в
водных растворах распадаются на частицы. Так,
водные растворы серной H 2 SO 4 , азотной HNO 3 ,
хлорной HClO 4 , хлороводородной (соляной) HCl,
уксусной CH 3 COOH и других кислот имеют кислый
вкус. В формулах кислот общей частицей является
атом водорода, и можно предположить, что он (в
виде иона) является причиной одинакового вкуса
всех этих столь различных веществ.
Образующиеся при диссоциации в водном растворе
ионы водорода придают раствору кислый вкус,
поэтому такие вещества и названы кислотами. В
природе только ионы водорода имеют кислый вкус.
Они создают в водном растворе так называемую
кислотную (кислую) среду.
Запомните, когда вы говорите «хлороводород», то имеете в виду газообразное и кристаллическое состояние этого вещества, но для водного раствора следует говорить «раствор хлороводорода», «хлороводородная кислота» или использовать общепринятое название «соляная кислота», хотя состав вещества в любом состоянии выражается одной и той же формулой – НСl.
Водные растворы гидроксидов лития (LiOH), натрия
(NаОН), калия (КОН), бария (Ва(ОН) 2), кальция
(Са(ОН) 2) и других металлов имеют одинаковый
неприятный горько-мыльный вкус и вызывают на
коже рук ощущение скольжения. По-видимому, за это
свойство ответственны гидроксид-ионы ОН – ,
входящие в состав таких соединений.
Хлороводородная HCl, бромоводородная HBr и
йодоводородная HI кислоты реагируют с цинком
одинаково, несмотря на свой различный состав, т.
к. в действительности с цинком реагирует не
кислота:
Zn + 2НСl = ZnСl 2 + Н2,
а ионы водорода:
Zn + 2H + = Zn 2+ + Н 2 ,
и образуются газообразный водород и ионы цинка.
Смешивание некоторых растворов солей, например
хлорида калия KCl и нитрата натрия NaNO 3 , не
сопровождается заметным тепловым эффектом, хотя
после выпаривания раствора образуется смесь
кристаллов четырех веществ: исходных – хлорида
калия и нитрата натрия – и новых – нитрата калия
КNO 3 и хлорида натрия NaCl. Можно предположить,
что в растворе две исходные соли полностью
распадаются на ионы, которые при его выпаривании
образуют четыре кристаллических вещества:
Сопоставляя эти сведения с
электропроводностью водных растворов кислот,
гидроксидов и солей и с рядом других положений,
С.А.Аррениус в 1887 г. выдвинул гипотезу
электролитической диссоциации, согласно которой
молекулы кислот, гидроксидов и солей при
растворении их в воде диссоциируют на ионы.
Изучение продуктов электролиза позволяет
приписать ионам положительные или отрицательные
заряды. Очевидно, если кислота, например азотная
НNO 3 , диссоциирует, предположим, на два иона
и при электролизе водного раствора на катоде
(отрицательно заряженный электрод) выделяется
водород, то, следовательно, в растворе имеются
положительно заряженные ионы водорода Н + .
Тогда уравнение диссоциации следует записать
так:
НNO 3 = Н + + .
Электролитическая диссоциация
–
полный или частичный распад соединения при его
растворении в воде на ионы в результате
взаимодействия с молекулой воды (или другого
растворителя).
Электролиты
– кислоты, основания или
соли, водные растворы которых проводят
электрический ток в результате диссоциации.
Вещества, не диссоциирующие в водном растворе на
ионы и растворы которых не проводят
электрический ток, называются неэлектролитами
.
Диссоциация электролитов количественно
характеризуется степенью диссоциации
– отношением числа распавшихся на ионы
«молекул» (формульных единиц) к общему числу
«молекул» растворенного вещества. Степень
диссоциации обозначается греческой буквой . Например, если из
каждых 100 «молекул» растворенного вещества 80
распадаются на ионы, то степень диссоциации
растворенного вещества равна: = 80/100 = 0,8, или 80%.
По способности к диссоциации (или, как говорят,
«по силе») электролиты разделяют на сильные
,
средние
и слабые
. По степени
диссоциации к сильным электролитам относят те из
них, для растворов которых > 30%, к слабым – < 3%, к средним – 3% 30%. Сила электролита –
величина, зависящая от концентрации вещества,
температуры, природы растворителя и др.
В случае водных растворов
к сильным электролитам
( > 30%) относят
перечисленные ниже группы соединений.
1
. Многие неорганические кислоты,
например хлороводородная НCl, азотная HNO 3 ,
серная H 2 SО 4 в разбавленных растворах.
Самая сильная неорганическая кислота – хлорная
НСlО 4 .
Сила некислородных кислот возрастает в ряду
однотипных соединений при переходе вниз по
подгруппе кислотообразующих элементов:
HCl – HBr – HI.
Фтороводородная (плавиковая) кислота HF растворяет стекло, но это вовсе не говорит о ее силе. Эта кислота из бескислородных галогенсодержащих относится к кислотам средней силы из-за высокой энергии связи Н–F, способности молекул HF к объединению (ассоциации) благодаря сильным водородным связям, взаимодействия ионов F – с молекулами НF (водородные связи) с образованием ионов и других более сложных частиц. В результате концентрация ионов водорода в водном растворе этой кислоты оказывается значительно пониженной, поэтому фтороводородную кислоту считают средней силы.
Фтороводород реагирует с диоксидом кремния, входящим в состав стекла, по уравнению:SiO 2 + 4HF = SiF 4 + 2H 2 O.
Фтороводородную кислоту нельзя хранить в стеклянных сосудах. Для этого используют сосуды из свинца, некоторых пластмасс и стекла, стенки которых покрыты изнутри толстым слоем парафина. Если для «травления» стекла использовать газообразный фтороводород, то поверхность стекла становится матовой, что используется для нанесения на стекло надписей и различных рисунков. «Травление» стекла водным раствором фтороводородной кислоты приводит к разъеданию поверхности стекла, которая остается прозрачной. В продаже обычно бывает 40%-й раствор плавиковой кислоты.
Сила однотипных кислородных кислот изменяется
в противоположном направлении, например йодная
кислота НIО 4 слабее хлорной кислоты НСlО 4 .
Если элемент образует несколько кислородных
кислот, то наибольшей силой обладает кислота, в
которой кислотообразующий элемент имеет самую
высокую валентность. Так, в ряду кислот НСlО
(хлорноватистая) – НСlО 2 (хлористая) – НСlО 3
(хлорноватая) – НСlО 4 (хлорная) последняя
наиболее сильная.
Один объем воды растворяет около двух объемов хлора. Хлор (примерно половина его) взаимодействует с водой:
Cl 2 + H 2 O = HCl + HСlO.
Хлороводородная кислота является сильной, в ее водном растворе практически нет молекул HCl. Правильнее уравнение реакции записать так:
Cl 2 + H 2 O = H + + Cl – + HClO – 25 кДж/моль.
Образующийся раствор называют хлорной водой.
Хлорноватистая кислота – быстродействующий окислитель, поэтому ее применяют для отбеливания тканей.
2 . Гидроксиды элементов главных подгрупп I и II групп периодической системы: LiОН, NaОН, КОН, Са(ОН) 2 и др. При переходе вниз по подгруппе по мере усиления металлических свойств элемента сила гидроксидов возрастает. Растворимые гидроксиды главной подгруппы I группы элементов относят к щелочам.
Щелочами называют растворимые в воде основания. К ним относят также гидроксиды элементов главной подгруппы II группы (щелочно-земельные металлы) и гидроксид аммония (водный раствор аммиака). Иногда щелочами считают те гидроксиды, которые в водном растворе создают высокую концентрацию гидроксид-ионов. В устаревшей литературе вы можете встретить в числе щелочей карбонаты калия К 2 СО 3 (поташ) и натрия Na 2 CO 3 (сода), гидрокарбонат натрия NaHCO 3 (питьевая сода), буру Na 2 B 4 O 7 , гидросульфиды натрия NaHS и калия KHS и др.
Гидроксид кальция Са(ОН) 2 как сильный электролит диссоциирует в одну ступень:
Са(ОН) 2 = Са 2+ + 2ОН – .
3 . Почти все соли. Соль, если это сильный электролит, диссоциирует в одну ступень, например хлорид железа:
FeCl 3 = Fe 3+ + 3Cl – .
В случае водных растворов к слабым электролитам ( < 3%) относят перечисленные ниже соединения.
1 . Вода H 2 O – важнейший электролит.
2
. Некоторые неорганические и почти
все органические кислоты: H 2 S
(сероводородная), H 2 SO 3 (сернистая), H 2 CO 3
(угольная), HCN (циановодородная), Н 3 РО 4
(фосфорная, ортофосфорная), H 2 SiO 3
(кремниевая), H 3 BO 3 (борная, ортоборная),
СН 3 СООН (уксусная) и др.
Заметим, что угольная кислота в формуле H 2 CO 3
не существует. При растворении углекислого газа
СО 2 в воде образуется его гидрат СО 2 Н 2 О,
который мы для удобства расчетов записываем
формулой H 2 CO 3 , и уравнение реакции
диссоциации выглядит так:
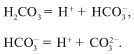
Диссоциация слабой угольной кислоты проходит в
две ступени. Образующийся гидрокарбонат-ион также ведет себя
как слабый электролит.
Точно так же ступенчато диссоциируют и другие
многоосновные кислоты: Н 3 РО 4
(фосфорная), H 2 SiO 3 (кремниевая), H 3 BO 3
(борная). В водном растворе диссоциация
практически проходит лишь по первой ступени. Как
осуществить диссоциацию по последней ступени?
3
. Гидроксиды многих элементов, например
Аl(OH) 3 , Cu(OH) 2 , Fe(OH) 2 , Fe(OH) 3 и др.
Все эти гидроксиды диссоциируют в водном
растворе ступенчато, например гидроксид железа
Fe(OH) 3:
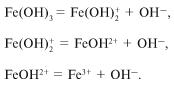
В водном растворе диссоциация проходит
практически только по первой ступени. Как
сместить равновесие в сторону образования ионов
Fe 3+ ?
Осно"вные свойства гидроксидов одного и того же
элемента усиливаются с уменьшением валентности
элемента. Так, осно"вные свойства дигидроксида
железа Fe(OH) 2 выражены сильнее, чем у
тригидроксида Fe(OH) 3 . Это утверждение
равносильно тому, что кислотные свойства Fe(OH) 3
проявляются сильнее, чем у Fe(OH) 2 .
4
. Гидроксид аммония NH 4 OH.
При растворении газообразного аммиака NH 3 в
воде получается раствор, который очень слабо
проводит электрический ток и имеет
горько-мыльный вкус. Среда раствора осно"вная,
или щелочная. Объясняется такое поведение
аммиака следующим образом. При растворении
аммиака в воде образуется гидрат аммиака NH 3 Н 2 О,
которому условно мы приписываем формулу
несуществующего гидроксида аммония NH 4 OH,
считая, что это соединение диссоциирует с
образованием иона аммония и гидроксид-иона ОН – :
NH 4 OH = + ОН – .
5 . Некоторые соли: хлорид цинка ZnCl 2 , тиоцианат железа Fe(NСS) 3 , цианид ртути Hg(CN) 2 и др. Эти соли диссоциируют ступенчато.
К электролитам средней силы некоторые относят фосфорную кислоту Н 3 РО 4 . Мы будем считать фосфорную кислоту слабым электролитом и записывать три ступени ее диссоциации. Серная кислота в концентрированных растворах ведет себя как электролит средней силы, а в очень концентрированных растворах – как слабый электролит. Мы далее будем считать серную кислоту сильным электролитом и записывать уравнение ее диссоциации в одну ступень.
Константа гидролиза равна отношению произведения концентраций
продуктов гидролиза к концентрации негидролизованной соли.
Пример 1. Вычислить степень гидролиза NH 4 Cl.
Решение: Из таблицы находим Кд(NH 4 ОН)=1,8∙10 -3 , отсюда
Кγ=Кв/Кд к = =10 -14 /1,8∙10 -3 = 5,56∙10 -10 .
Пример 2. Вычислить степень гидролиза ZnCl 2 по 1 ступени в 0,5 М растворе.
Решение: Ионное уравнение гидролиза Zn 2 + H 2 O ZnOH + + H +
Kд ZnOH +1=1,5∙10 -9 ; hγ=√(Кв/ [Кд осн ∙Cм]) = 10 -14 /1,5∙10 -9 ∙0,5=0,36∙10 -2 (0,36%).
Пример 3. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: a) KCN; б) Na 2 CO 3 ; в) ZnSO 4 . Определите реакцию среды растворов этих солей.
Решение: а) Цианид калия KCN - соль слабой одноосновной кислоты (см. табл. I приложения) HCN и сильного основания КОН. При растворении в воде молекулы KCN полностью диссоциируют на катионы К + и анионы CN - . Катионы К + не могут связывать ионы ОН - воды, так как КОН - сильный электролит. Анионы же CN - связывают ионы Н + воды, образуя молекулы слабого элекролита HCN. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CN - + Н 2 О HCN + ОН -
или в молекулярной форме
KCN + Н 2 О HCN + КОН
В результате гидролиза в растворе появляется некоторый избыток ионов ОН - , поэтому раствор KCN имеет щелочную реакцию (рН > 7).
б) Карбонат натрия Na 2 CO 3 - соль слабой многоосновной кислоты и сильного основания. В этом случае анионы соли СО 3 2- , связывая водородные ионы воды, образуют анионы кислой соли НСО - 3 , а не молекулы Н 2 СО 3 , так как ионы НСО - 3 диссоциируют гораздо труднее, чем молекулы Н 2 СО 3 . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза
CO 2- 3 +H 2 O HCO - 3 +ОН -
или в молекулярной форме
Na 2 CO 3 + Н 2 О NaHCO 3 + NaOH
В растворе появляется избыток ионов ОН - , поэтому раствор Na 2 CO 3 имеет щелочную реакцию (рН > 7).
в) Сульфат цинка ZnSO 4 - соль слабого многокислотного основания Zn(OH) 2 и сильной кислоты H 2 SO 4 . В этом случае катионы Zn + связывают гидроксильные ионы воды, образуя катионы основной соли ZnOH + . Образование молекул Zn(OH) 2 не происходит, так как ионы ZnOН + диссоциируют гораздо труднее, чем молекулы Zn(OH) 2 . В обычных условиях гидролиз идет по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза
Zn 2+ + Н 2 О ZnOН + + Н +
или в молекулярной форме
2ZnSO 4 + 2Н 2 О (ZnOH) 2 SO 4 + H 2 SO 4
В растворе появляется избыток ионов водорода, поэтому раствор ZnSO 4 имеет кислую реакцию (рН < 7).
Пример 4. Какие продукты образуются при смешивании растворов A1(NO 3) 3 и К 2 СО 3 ? Составьте ионно-молекулярное и молекулярное уравнение реакции.
Решение. Соль A1(NO 3) 3 гидролизуется по катиону, а К 2 СО 3 - по аниону:
А1 3+ + Н 2 О А1ОН 2+ + Н +
СО 2- 3 + Н 2 О НСО - з + ОН -
Если растворы этих солей находятся в одном сосуде, то идет взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН - образуют молекулу слабого электролита Н 2 О. При этом гидролитическое равновесие сдвигается вправо и гидролиз каждой из взятых солей идет до конца с образованием А1(ОН) 3 и СО 2 (Н 2 СО 3). Ионно-молекулярное уравнение:
2А1 3+ + ЗСО 2- 3 + ЗН 2 О = 2А1(ОН) 3 + ЗСО 2
молекулярное уравнение: ЗСО 2 + 6KNO 3
2A1(NO 3) 3 + ЗК 2 СО 3 + ЗН 2 О = 2А1(ОН) 3
1. ЭЛЕКТРОЛИТЫ
1.1. Электролитическая диссоциация. Степень диссоциации. Сила электролитов
Согласно теории электролитической диссоциации, соли, кислоты, гидроксиды, растворяясь в воде, полностью или частично распадаются на самостоятельные частицы – ионы.
Процесс распада молекул веществ на ионы под действием полярных молекул растворителя называют электролитической диссоциацией . Вещества, диссоциирующие на ионы в растворах, называют электролитами. В результате раствор приобретает способность проводить электрический ток, т.к. в нем появляются подвижные носители электрического заряда. Согласно этой теории, при растворении в воде электролиты распадаются (диссоциируют) на положительно и отрицательно заряженные ионы. Положительно заряженные ионы называют катионами ; к ним относятся, например, ионы водорода и металлов. Отрицательно заряженные ионы называются анионами ; к ним принадлежат ионы кислотных остатков и гидроксид-ионы.
Для количественной характеристики процесса диссоциации введено понятие степени диссоциации. Степенью диссоциации электролита (α) называется отношение числа его молекул, распавшихся в данном растворе на ионы (n ), к общему числу его молекул в растворе (N ), или
α = .
Степень электролитической диссоциации принято выражать либо в долях единицы, либо в процентах.
Электролиты со степенью диссоциации больше 0,3 (30%) обычно называют сильными, со степенью диссоциации от 0,03 (3%) до 0,3 (30%)-средними, менее 0,03 (3%)-слабыми электролитами. Так, для 0,1 M раствора CH 3 COOH α = 0,013 (или 1,3 %). Следовательно, уксусная кислота является слабым электролитом. Степень диссоциации показывает, какая часть растворенных молекул вещества распалась на ионы. Степень электролитической диссоциации электролита в водных растворах зависит от природы электролита, его концентрации и температуры.
По своей природе электролиты можно условно разделить на две большие группы: сильные и слабые . Сильные электролиты диссоциируют практически полностью (α = 1).
К сильным электролитам относятся:
1) кислоты (H 2 SO 4 , HCl , HNO 3 , HBr , HI , HClO 4 , H М nO 4 );
2) основания – гидроксиды металлов первой группы главной подгруппы (щелочи) – LiOH , NaOH , KOH , RbOH , CsOH , а также гидроксиды щелочноземельных металлов – Ba (OH ) 2 , Ca (OH ) 2 , Sr (OH ) 2 ;.
3) соли, растворимые в воде (см. таблицу растворимости).
Слабые электролиты диссоциируют на ионы в очень малой степени, в растворах они находятся, в основном в недиссоциированном состоянии (в молекулярной форме). Для слабых электролитов устанавливается равновесие между недиссоциированными молекулами и ионами.
К слабым электролитам относятся:
1) неорганические кислоты (H 2 CO 3 , H 2 S , HNO 2 , H 2 SO 3 , HCN , H 3 PO 4 , H 2 SiO 3 , HCNS , HСlO и др.);
2) вода (H 2 O );
3) гидроксид аммония (NH 4 OH );
4) большинство органических кислот
(например, уксусная CH 3 COOH, муравьиная HCOOH);
5) нерастворимые и малорастворимые соли и гидроксиды некоторых металлов (см. таблицу растворимости).
Процесс электролитической диссоциации изображают, пользуясь химическими уравнениями. Например, диссоциация соляной кислоты (НС l ) записывается следующим образом:
HCl → H + + Cl – .
Основания диссоциируют с образованием катионов металла и гидроксид-ионов. Например, диссоциация КОН
КОН → К + + ОН – .
Многоосновные кислоты, а также основания многовалентных металлов диссоциируют ступенчато. Например,
H 2 CO 3 H + + HCO 3 – ,
HCO 3 – H + + CO 3 2– .
Первое равновесие – диссоциация по первой ступени – характеризуется константой
![]() .
.
Для диссоциации по второй ступени:
![]() .
.
В случае угольной кислоты константы диссоциации имеют следующие значения: K I = 4,3 × 10 –7 , K II = 5,6 × 10 –11 . Для ступенчатой диссоциации всегда K I >K II >K III > ... , т.к. энергия, которую необходимо затратить для отрыва иона, минимальна при отрыве его от нейтральной молекулы.
Средние (нормальные) соли, растворимые в воде, диссоциируют с образованием положительно заряженных ионов металла и отрицательно заряженных ионов кислотного остатка
Ca(NO 3) 2 → Ca 2+ + 2NO 3 –
Al 2 (SO 4) 3 → 2Al 3+ +3SO 4 2– .
Кислые соли (гидросоли) – электролиты, содержащие в анионе водород, способный отщепляться в виде иона водорода Н + . Кислые соли рассматривают как продукт, получающийся из многоосновных кислот, в которых не все атомы водорода замещены на металл. Диссоциация кислых солей происходит по ступеням, например:
KHCO 3 → K + + HCO 3 – (первая ступень)
Все вещества можно разделить на электролиты и неэлектролиты. К электролитам относятся вещества, растворы или расплавы которых проводят электрический ток (например, водные растворы или расплавы KCl, H 3 PO 4 , Na 2 CO 3). Вещества неэлектролиты при расплавлении или растворении электрический ток не проводят (сахар, спирт, ацетон и др.).
Электролиты подразделяются на сильные и слабые. Сильные электролиты в растворах или расплавах полностью диссоциируют на ионы. При написании уравнений химических реакций это подчеркивается стрелкой в одном направлении, например:
HCl→ H + + Cl -
Ca(OH) 2 → Ca 2+ + 2OH -
К сильным электролитам относятся вещества с гетерополярной или ионной кристаллической структурой (таблица 1.1).
Таблица 1.1 Сильные электролиты
Слабые электролиты на ионы распадаются лишь частично. Наряду с ионами в расплавах или растворах данных веществ присутствуют в подавляющем большинстве недиссоциированные молекулы. В растворах слабых электролитов параллельно с диссоциацией протекает обратный процесс - ассоциация, т.е соединение ионов в молекулы. При записи уравнения реакции это подчеркивается двумя противоположно направленными стрелками.
CH 3 COOH D CH 3 COO - + H +
К слабым электролитам относятся вещества с гомеополярным типом кристаллической решетки (таблица 1.2).
Таблица 1.2 Слабые электролиты
Равновесное состояние слабого электролита в водном растворе количественно характеризуют степенью электролитической диссоциации и константой электролитической диссоциации.
Степень электролитической диссоциации α представляет собой отношение числа молекул, распавшихся на ионы, к общему числу молекул растворенного электролита:
Степень диссоциации показывает, какая часть от общего количества растворенного электролита распадается на ионы и зависит от природы электролита и растворителя, а также от концентрации вещества в растворе, имеет безразмерную величину, хотя обыкновенно ее выражают в процентах. При бесконечном разбавлении раствора электролита степень диссоциации приближается к единице, что соответствует полной, 100%-ной, диссоциации молекул растворенного вещества на ионы. Для растворов слабых электролитов α <<1. Сильные электролиты в растворах диссоциируют полностью (α =1). Если известно, что в 0,1 М растворе уксусной кислоты степень электрической диссоциации α =0,0132, это означает, что 0,0132 (или 1,32%) общего количества растворённой уксусной кислоты продиссоциировало на ионы, а 0,9868 (или 98,68%) находится в виде недиссоциированных молекул. Диссоциация слабых электролитов в растворе подчиняется закону действия масс.
В общем виде обратимую химическую реакцию можно представить как:
a A + b B D d D + e E
Скорость реакции прямо пропорциональна произведению концентрации реагирующих частиц в степенях их стехиометрических коэффициентов. Тогда для прямой реакции
V 1 =k 1 [A] a [B] b ,
а скорость обратной реакции
V 2 =k 2 [D] d [Е] е.
В некоторый момент времени скорости прямой и обратной реакции выровняются, т.е.
Такое состояние называют химическим равновесием. Отсюда
k 1 [A] a [B] b = k 2 [D] d [Е] е
Сгруппировав постоянные величины с одной стороны, а переменные- с другой стороны, получим:
Таким образом, для обратимой химической реакции в состоянии равновесия произведение равновесных концентраций продуктов реакции в степенях их стехиометрических коэффициентов, отнесенное к такому же произведению для исходных веществ есть величина постоянная при данных температуре и давлении. Численное значение константы химического равновесия К не зависит от концентрации реагирующих веществ. Например, константу равновесия диссоциации азотистой кислоты в соответствии с законом действия масс можно записать в виде:
HNO 2 + H 2 OD H 3 O + + NO 2 -
Величину К а называют константой диссоциации кислоты, в данном случае азотистой.
Аналогично выражается и константа диссоциации слабого основания. Например, для реакции диссоциации аммиака:
NH 3 + H 2 O DNH 4 + + OH -
Величину К b называют константой диссоциации основания, в данном случае аммиака. Чем выше константа диссоциации электролита, тем сильнее электролит диссоциирует и тем выше концентрации его ионов в растворе при равновесии. Между степенью диссоциации и константой диссоциации слабого электролита существует взаимосвязь:
Это математическое выражение закона разбавления Оствальда: при разбавлении слабого электролита степень его диссоциации увеличивается.Для слабых электролитов при К ≤1∙ 10 -4 и С ≥0,1 моль/л используют упрощенное выражение:
К = α 2 ∙С или α
Пример1 . Вычислите степень диссоциации и концентрацию ионов и [ NH 4 + ] в 0,1 М растворе гидроксида аммония, если К NH 4 OH =1,76∙10 -5
Дано: NH 4 OH
К NH 4 OH =1,76∙10 -5
Решение :
Так как электролит является достаточно слабым (К NH 4 OH =1,76∙10 –5 <1∙ 10 - 4) и раствор его не слишком разбавлен, можно принять, что:
или 1,33%
Концентрация ионов в растворе бинарного электролита равна C ∙α, так как бинарный электролит ионизирует с образованием одного катиона и одного аниона, то = [ NH 4 + ]=0,1∙1,33∙10 -2 =1,33∙10 -3 (моль/л).
Ответ: α=1,33 %; = [ NH 4 + ]=1,33∙10 -3 моль/л.
Теория сильных электролитов
Сильные электролиты в растворах и расплавах полностью диссоциируют на ионы. Однако экспериментальные исследования электропроводности растворов сильных электролитов показывают, что ее величина несколько занижена по сравнению с той электропроводностью, которая должна бы быть при 100 % диссоциации. Такое несоответствие объясняется теорией сильных электролитов, предложенной Дебаем и Гюккелем. Согласно этой теории, в растворах сильных электролитов между ионами существует электростатическое взаимодействие. Вокруг каждого иона образуется “ионная атмосфера” из ионов противоположного знака заряда, которая тормозит движение ионов в растворе при пропускании постоянного электрического тока. Кроме электростатического взаимодействия ионов, в концентрированных растворах нужно учитывать ассоциацию ионов. Влияние межионных сил создает эффект неполной диссоциации молекул, т.е. кажущейся степени диссоциации. Определенная на опыте величина α всегда несколько ниже истинной α. Например, в 0,1 М растворе Na 2 SO 4 экспериментальная величина α =45 %. Для учета электростатических факторов в растворах сильных электролитов пользуются понятием активности (а). Активностью иона называют эффективную или кажущуюся концентрацию, согласно которой ион действует в растворе. Активность и истинная концентрация связаны между собой выражением:
где f – коэффициент активности, который характеризует степень отклонения системы от идеальной из-за электростатических взаимодействий ионов.
Коэффициенты активности ионов зависят от величины µ, называемой ионной силой раствора. Ионная сила раствора является мерой электростатического взаимодействия всех ионов, присутствующих в растворе и равнаполовине суммы произведений концентраций (с) каждого из присутствующих в растворе ионов на квадрат его зарядового числа (z) :
В разбавленных растворах (µ<0,1М) коэффициенты активности меньше единицы и уменьшаются с ростом ионной силы. Растворы с очень низкой ионной силой (µ < 1∙10 -4 М) можно считать идеальными. В бесконечно разбавленных растворах электролитов активность можно заменить истинной концентрацией. В идеальной системе a = c и коэффициент активности равен 1. Это означает, что электростатические взаимодействия практически отсутствуют. В очень концентрированных растворах (µ>1М) коэффициенты активности ионов могут быть больше единицы. Связь коэффициента активности с ионной силой раствора выражается формулами:
При µ <10 -2
При 10 -2 ≤ µ ≤ 10 -1
0,1z 2 µ при 0,1<µ <1
Константа равновесия, выраженная через активности, называется термодинамической. Например, для реакции
a A + b B d D + e E
термодинамическая константа имеет вид:
Она зависит от температуры, давления и природы растворителя.
Поскольку активность частицы , то
где К С - концентрационная константа равновесия.
Значение К С зависит не только от температуры, природы растворителя и давления, но и от ионной силы m . Так как термодинамические константы зависят от наименьшего числа факторов то, следовательно, являются наиболее фундаментальными характеристиками равновесия. Поэтому в справочниках приводятся именно термодинамические константы. Величины термодинамических констант некоторых слабых электролитов приведены в приложении данного пособия. =0,024 моль/л.
С ростом заряда иона коэффициент активности и активность иона уменьшается.
Вопросы для самоконтроля:
- Что такое идеальная система? Назовите основные причины отклонения реальной системы от идеальной.
- Что называют степенью диссоциации электролитов?
- Приведите примеры сильных и слабых электролитов.
- Какая взаимосвязь существует между константой диссоциации и степенью диссоциации слабого электролита? Выразите её математически.
- Что такое активность? Как связаны активность иона и его истинная концентрация?
- Что такое коэффициент активности?
- Как влияет заряд иона на величину коэффициента активности?
- Что такое ионная сила раствора, ее математическое выражение?
- Запишите формулы для расчета коэффициентов активности индивидуальных ионов в зависимости от ионной силы раствора.
- Сформулируйте закон действия масс и выразите его математически.
- Что такое термодинамическая константа равновесия? Какие факторы влияют на ее величину?
- Что такое концентрационная константа равновесия? Какие факторы влияют на ее величину?
- Как связаны термодинамическая и концентрационная константы равновесия?
- В каких пределах могут изменяться величины коэффициента активности?
- В чем заключаются основные положения теории сильных электролитов?